Tratamiento
OBJETIVO TERAPÉUTICO
Erradicación de la infección por VHC, evidenciado por la negativización del ARN VHC 24 semanas después de finalizado el tratamiento antiviral (respuesta virológica sostenida-RVS).
APROXIMACIÓN GENERAL
Indicación:
- ARN VHC circulante sérico.
- Daño hepático histológico de moderado a severo.
- Enfermedad hepática compensada.
Contraindiciones

Determinaciones antes de iniciar el tratamiento:
- Cuantificación del ARN VHC sérico: carga viral basal que permite valorar la cinética viral.
- Genotipo viral: determina el tipo de tratamiento farmacológico y pronóstico de respuesta.
- Grado de fibrosis: mediante biopsia o elastografía, para decidir inicio del tratamiento.
Definiciones de respuesta al tratamiento:
- Respuesta virológica rápida (RVR): CVP VHC indetectable a la semana 4.
- Respuesta virológica temprana (RVT):
- RVT parcial: al menos una reducción de 2 log de la CVP VHC a la semana 12.
- RVT completa: CVP VHC indetectable en la semana 12.
- Respuesta virológica final (RVF): CVP VHC indetectable al final del tratamiento.
- Respuesta viral sostenida (RVS): CVP VHC al final y hasta 24 semanas posteriores del tratamiento.
Estratificación de pacientes:
- Recaedor: paciente con RVF pero sin RVS.
- No respondedor: paciente con CVP VHC detectable a la semana 24.
- Respondedor nulo: paciente sin disminución CVP VHC > 2 log a la semana 24.
- Respondedor Parcial: paciente con disminución CVP VHC ≥ 2 log pero detectable a la semana 24.
Factores predictivos positivos de RVS en relación a la cinética de eliminación viral:
- RVR.
- RVT.
TERAPIA NO FARMACOLÓGICA
- Vacunación frente a hepatitis A y B.
- Supresión consumo de alcohol y tabaco.
- Normalización del peso corporal.
TERAPIA FARMACOLÓGICA
Estándar de tratamiento:
Asociar los siguientes medicamentos
- Inyección subcutánea semanal de interferón pegilado:
- Peginterferón alfa-2a 180 mcg/semana ó Peginterferón alfa-2b 1,5 mcg/kg peso paciente.
- Dosis oral diaria de ribavirina (RBV):
- 800 – 1400 mg/día, según peso del paciente
- Dosis oral diaria de un inhibidor de proteasa (sólo si VHC es genotipo 1):
- Boceprevir(BOC): 800 mg/8 horas.
- Telaprevir (TEL): 1125 mg/12 horas ó 750 mg/8 horas.
- Duración general de tratamiento:
- 48 semana para genotipos 1,4,5, 6.
- 24 semanas para genotipos 2, 3.
Elementos de Optimización de la terapia farmacológica:
- Genotipo viral.
- Tipo de paciente, estratificado según respuesta previa.
- Peso inicial del paciente.
- Cinética de eliminación viral.
PACIENTES SIN TRATAMIENTO PREVIO. GENOTIPO 1 DEL VHC.
Tratamiento de elección: boceprevir o telapreviren combinación con peginterferón alfa y ribavirina.
- BOC+PegIFNα+RBV durante 24-44 semanas, precedidos por 4 semanas sin BOC:
- Pacientes sin cirrosis: considerar 28 semanas si ARN VHC es indetectable a las semana 8 y 24.
- Suspender los tres medicamentos si ARN del VHC es > 100 UI / mL a la semana 12 o detectable a la semana de tratamiento 24.
- TEL+PegIFNα+RBV durante 12 semanas, seguidas de 12-36 semanas sin TEL.
- Pacientes sin cirrosis: considerar 24 semanas si ARN VHC es indetectable a las semana 4 y 12.
- Suspender los tres medicamentos si ARN VHC es > 1.000 UI / mL a la semana 4 ó 12 o detectable a la semana 24.
Pacientes cirróticos: triple terapia durante 48 semanas.
PACIENTES CON TRATAMIENTO PREVIO. GENOTIPO 1 DEL VHC.
Tratamiento de elección: boceprevir o telaprevir en combinación con peginterferón alfa y ribavirina:
- Recaedores.
- Respondedor parcial.
- Respondedores nulos.
GENOTIPO 4 DEL VHC.
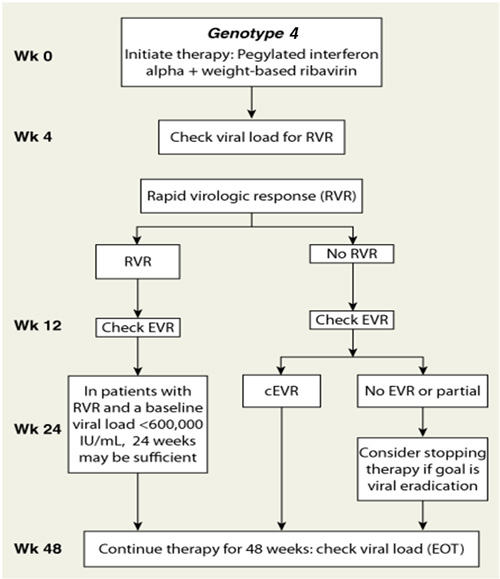
GENOTIPOS 2,3 DEL VHC.
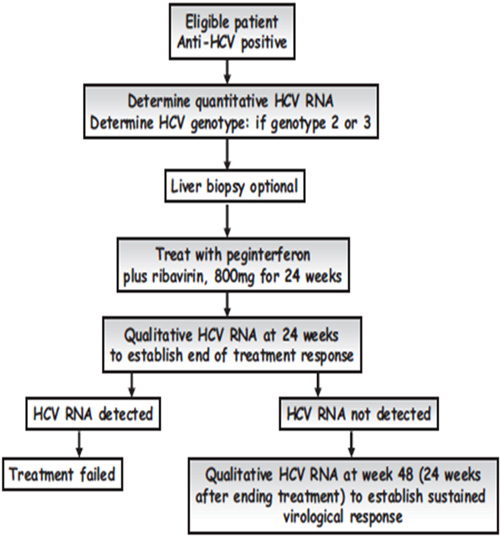
Peg-Interferón (PegIFN):
- La pegilación de la molécula de interferón ha permitido la administración semanal y duplicó RVS.
- Disponibles: PegIFN alfa-2a y PegIFN alfa-2b.
Ribavirina:
- Análogo de guanosina sintético, ineficaz como monoterapia y mecanismo de acción desconocido.
- Asociado a PegIFN, aumenta significativamente la RVS.
- Dosificación según peso corporal en genotipos 1 y 4.
EFECTOS ADVERSOS
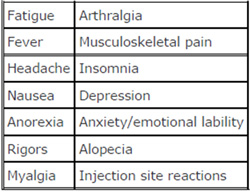
Frecuentes y graves, provocando reducciones de dosis y suspensiones de tratamiento.
Fatiga y síndrome pseudogripal.
Anemia, neutropenia y trombocitopenia.
Ribavirina: provoca anemia hemolítica y requiere reducción de dosis si la hemoglobina sérica es inferior a 10 g/l, normalizándose tras suspensión.
PegIFN: neutropenia y trombocitopenia. Se recomienda disminuir dosis si el recuento de neutrófilos <750 células/mm y suspender si <500 células/mm. No hay un mayor riesgo de infección.
Depresión: hasta un tercio de los pacientes secundario a PegIFN, tratable con inhibidores de la recaptación de serotonina.
Telaprevir: exantema, anemia, prurito, síntomas anales, náuseas y diarrea.
Boceprevir: anemia, disgéusia.
POBLACIONES ESPECIALES
Pacientes con ALTs normales.
- Decisión individualizada, valorando los riesgos y beneficios del tratamiento.
Cirrosis descompensada.
- Pacientes candidatos a trasplante hepático.
- Tratamiento no recomendado.
Pinchazo accidental con agujas.
- No recomendado el tratamiento, por bajo riesgo de transmisión y, en su caso, seroconversión.
Usuarios de drogas por vía parenteral.
- Decisión de tratamiento individualizada.
- Recomendado en pacientes en terapia de recuperación.
Alcoholismo.
- Tratamiento no recomendado si el paciente es alcohólico activo.
Enfermedad renal terminal.
- Contraindica el uso de ribavirina debido al elevado riesgo de anemia hemolítica.
VIH-SIDA.
- Alta prevalencia de la coinfección:
- solapamiento toxicidad hepática de los antirretrovirales.
- complicaciones hepáticas de enfermedades asociadas con el VIH.
- reactivación hepatitis al incrementarse el recuento de CD4.
- Mismas recomendaciones que en monoinfectados, excepto en genotipo 1 en los que no se encuentra autorizados los inhibidores de proteasa, por lo que se trata como un genotipo 4.
- Contraindicada la coadministración de zidovudina y didanosina.
Niños.
- Indicada para niños > 2 años con PegIFN alfa-2b y ribavirina durante 48 semanas.


